NYERIKANKER
Nyeri kanker merupakan komplikasi
kanker yang paling sering ditemui pada
pasien kanker. Frekuensinya sekitar 30-
50% pada pasien yang sedang menjalani
terapi dan meningkat hingga 70-90% pada
kanker tahap lanjut. Oleh karena sifat
nyerinya yang bisa memberat secara terus
menerus dalam jangka waktu yang lama,
maka pasien dapat mengalami gangguan
tidur dan nafsu makan hingga depresi. Tak
heran bahwa nyeri kanker menjadi sangat
ditakuti oleh penderitanya dan merupakan
salah satu target pada terapi kanker secara
keseluruhan. National Comprehensive
Cancer Network (NCCN) dalam Panduan
Nyeri Kanker 2016 menyatakan bahwa
kesintasan penderita berhubungan erat
dengan manajemen gejala kanker yang baik,
termasuk manajemen nyeri kanker, dalam
meningkatkan kualitas hidup.
Keluhan nyeri ini dapat dirasakan dalam
setiap fase perkembangan kanker (Gambar
1), mulai dari fase penegakan Diagnosa
ataupun staging, fase kemoterapi, fase
pembedahan, fase remisi, fase relaps,
ataupun fase kesintasan (survivorship).
Sindrom nyeri kanker dapat dibagi secara
luas menjadi tipe akut dan kronik. Sindrom
nyeri kanker akut biasanya ditemukan
dalam proses diagnostik atau terapi
intervensi, sedangkan pada yang kronik
berhubungan langsung dengan kanker itu
sendiri atau terapi antineoplastik.
EPIDEMIOLOGI
WHO World Cancer Report 2014
menunjukkan angka insidens kejadian
Diagnosa kanker baru dan angka kematian
akibat kanker yang tinggi dan diperkirakan
meningkat sebanyak 70% dalam dua dekade
ke depan. Sebanyak 70% pasien kanker
dapat mengeluhkan keluhan nyeri, yaitu 30-
50% pada suatu saat dalam terapi hingga
90% pada stadium kanker lanjut.
PATOFISIOLOGI
Pada awalnya, nyeri kanker dapat berhubungan dengan terapi kanker itu sendiri, misalnya
prosedur bedah terkait biopsi diagnostik
atau terapi, efek samping obat kemoterapi,
dan terapi radiasi. Seiring perjalanan penyakit, nyeri kanker akan semakin intens. Hal ini
disebabkan oleh kerusakan nosiseptor akibat
pertumbuhan tumor. Selain itu, nosiseptor
juga menjadi tersensitisasi oleh penglepasan
faktor-faktor dari sel kanker dan sel stromal,
misalnya nerve growth factor. Bila perjalanan
penyakit kanker terus berlanjut, maka terjadi
proses pembentukan nerve sprouting ektopik
dan neuroma. Hal ini yaitu salah satu faktor
yang mendasari terjadinya nyeri sontak pada
pasien kanker (Gambar 1).
Evolusi nyeri kanker semng perjalanan
penyakitnya ini tidak lepas dari patofisiologi
dari nyeri kanker. Ada pun patofisiologi nyeri
kanker terdiri dari beberapa proses, yaitu:
1. Faktor-faktor Sel Tumor
Sel tumor mensekresi berbagai faktor yang
diperlukan untuk pertumbuhannya, seperti bradikinin, kanabinoid, endotelin, interleukin-6 (IL-6), granulocyte-macrophage
colony-stimulating factor (GM-CSF), nerve
growth factors (NGF), protease, dan tumor
necrosis factor-a (TNF-a), yang merangsang reseptor nyeri (Gambar 2).
2. Asidosis Jaringan Terinduksi Sel Tumor
Sel kanker secara umum mempunyai
pH yang rendah (6,8) jika dibandingkan
dengan sel normal (pH 7,2) akibat sekresi
asam laktat hasil glikolisis anaerob.
Jaringan sekitar tumor dengan pH rendah
ini akan mengaktifkan ujung serabut
saraf sensori bebas dan mengaktifkan
transient receptor potential vanilloid 1
(TRPVl) atau reseptor kapsaisin. Sensasi
sensorik yang ditimbulkan yaitu rasa
panas di daerah jaringan tumor.
Massa kanker memiliki komposisi sel-sel
inflamasi dan pembuluh darah yang sering
berdekatan dengan nosiseptor. Sel kanker
dan sel inflamasi ini melepaskan
berbagai sitokin, seperti adenosine
SI?J-triphosphate (ATP), bradikinin, W, nerve
growth factor (NGF), prostaglandin, dan
vascular endothelial growth factor (VEGF)
yang bisa mengeksitasi atau sensitisasi
nosiseptor. Stimulus nyeri ini
dihantarkan oleh saraf perifer melalui
ganglion radiks dorsalis menuju medula
spinalis dan pusat yang lebih tinggi di
otak. Aktivasi nosiseptor memicu
penglepasan neurotransmiter, antara lain
calcitonin gene-related peptide (CRGP),
endotelin, histamin, glutamat, dan substansi
. Selain itu, terjadi juga penglepasan
prostaglandin dari ujung terminal saraf
sensorik, sehingga dapat menginduksi
ekstravasasi plasma, aktivasi sel-sel imun,
dan vasodilatasi.
3. Instabilitas Mekanik Skeletal
Terinduksi Sel Tumor
Tulang merupakan daerah yang sering
mengalami metastasis. Untuk menyiapkan tempat tumbuhnya, sel kanker merangsang osteoblas mengekspresikan activator
of nuclear factor kappa-B (RANK) dan osteoprotegerin (OPG). RANKL kemudian
berikatan dengan ligannya (RANKL),
sehingga terjadi pematangan osteoklas.
Interaksi OPG dengan RANKL akan me-
643
ningkatkan resoprsi tulang. Peningkatan
osteoklas yang matang juga memicu tulang melepaskan insulin growth
factor (IGF)-1 dan tumor growth factor
(TGF)-~ yang akan mengaktifkan jalur
kaskade seperti sebelumnya, sehingga
terjadi proses resorpsi tulang terusmenerus (Gambar 3).
Sel kanker juga menghasilkan sitokin,
seperti IL-6, IL-11, prostaglandin
E2, dan tumor necrosis factor alpha
(TNF-a), yang berperan menginduksi
pembentukan osteoklas dan supresi
osteoblas. Sementara prostaglandin E2
meningkatkan pembentukan osteoklas
dengan menambah . jumlah produksi
RANKL. Aktivasi osteoklas ini
memicu destruksi tulang, sehingga
mengaktifkan sera but saraf be bas dalam
tulang dan terjadi penekanan serta
edema pada jaringan sekitarnya yang
menimbulkan nyeri hebat saat bergerak
atau menyangga beban dan instabilitas
mekanik tulang.
4. Kerusakan Sel Saraf Akibat Tumor
dan Nyeri Neuropatik
Sel tumor dan sel stromal dapat menginfiltrasi jaringan ikat di sekitarnya yang
mengandung serabut saraf bebas. Sel
abnormal ini akan menhancurkan bagian distal dari serabut saraf sensoris
bebas, dan sejalan dengan waktu akan
memicu diskontinuitas dan frag-
644
mentasi sel saraf. Selain itu, sel saraf ini
juga dapat mengalami kerusakan akibat
kemoterapi, pembedahan, atau radiasi.
Pad a metastasis ke tulang vertebra dapat
terjadi fraktur kompresi yang memicu kerusakan pedikel dan menekan
radiks, sehingga menimbulkan nyeri radikular.
5. Formasi Neuroma dan Pertumbuhan
Saraf Terinduksi Sel Tumor
Sel tumor dan sel stromal dapat
menginduksi pertumbuhan abnormal
serabutsarafbebas dan formasi neuroma.
Hal ini menimbulkan perubahan fenotip
sensoris dan serabut saraf simpatis,
termasuk ketidakseimbangan saluran
ion Natrium, sehingga memicu
eksitasi spontan dan cetusan ektopik
terkait pergerakan, yang dirasakan
sebagai rasa nyeri.
6. Proses Sensitisasi Sentral
Pada nyeri kanker terjadi reorganisasi
struktur yang signifikan di susunan
saraf tepi dan pusat akibat perubahan
komunikasi dari struktur saraf itu
sendiri. Sebagai contoh, mediator kimia
yang dilepas oleh sel glia- teraktifasi
nyeri terus menerus dapat mengontrol
amplituda respons sinaptik dengan
mengubah tingkat ekspresi reseptor
N-methyl-D-aspartate (NMDA) dan
alpha-amino-3-hydroxy-5-methyl-4-
isoxazolepropionic acid (AMPA), serta
fosforilasi keduanya.
GEJALA KLINIS
Gejala nyeri yang dialami oleh pasien harus
dipahami berdasar karakteristik nyeri,
seperti intensitas, kualitas, distribusi, dan
hubungan waktu antar kejadian nyeri
(temporal relationship). Evaluasi intensitas
nyeri merupakan hal penting karena
menentukan jenis terapi.
Kualitas nyeri menyiratkan patofisiologi
yang mendasarinya (Tabel 1). Nyeri
nosiseptif somatik biasanya dapat
dilokalisasi, terasa tajam, seperti ditusukNyeri Kanker
tusuk, atau tertekan (pressure-like). Nyeri
nosiseptif viseral bersifat difus dan sulit
dilokalisasi. Bila nyeri ini terjadi karena
obstruksi suatu rongga tubuh, maka
keluhannya dapat berupa kram atau kolik.
Nyeri neuropatik dideskripsikan sebagai
rasa terbakar, kesemutan, atau seperti
kesetrum listrik (shock-like).
Distribusi nyeri kanker biasanya lebih dari
satu tempat, sehingga perlu ditentukan
antara fokal, multifokal, dan generalisata.
Hal ini berhubungan dengan terapi yang
diambil, yaitu blok saraf, radioterapi, atau
operasi bedah. Nyeri terdistribusi fokal hila
terjadi hanya pada satu tempat, biasanya di
tempat lesi. Nyeri fokal ini perlu dibedakan
dengan nyeri rujuk, yaitu sumber nyeri
- berasal dari tempat yang berbeda dengan lesi
patologisnya, seperti nyeri daerah nasofaring
yang dapat terasa di puncak kepala.
645
Evaluasi waktu kejadian nyeri dapat
menunjukkan nyeri tergolong akut atau
kronik. Pasien dengan nyeri akut biasanya
disertai perilaku nyeri yang nyata, seperti
mengerang, meringis, dan cenderung
tidak mau bergerak. Selain itu, ada
rasa cemas, berkeringat ( diaforesis ), dan
berdebar-debar. Berbeda dengan nyeri akut,
pasien dengan nyeri kanker kronik biasanya
mengalami gangguan afektif, misalnya
depresi. Selain itu, pasien terlihat kurus,
nafsu makan menurun, dan gangguan tidur.
Selain nyeri akut dan kronik ada pula
nyeri sontak. Nyeri ini dirasa tajam dan
hebat, dengan pola eksaserbasi transien
di antara nyeri dasar yang terkontrol, baik
pada nyeri kanker akut maupun kronik.
Nyeri sontak dapat ditimbulkan pada
keadaan gerak disadari pasien (seperti pada
pergerakan, batuk, berkemih, dan defekasi)
maupun pada gerak yang tidak disadari
(gerakan motilitas usus). Nyeri sontak
ini dapat berdurasi dalam hitungan detik
ataupunjam (1-240 menit).
Pada nyeri akibatmetastasis tulangvertebra,
nyeri biasanya dimulai dengan nyeri lokal
yang dikatakan pasien sebagai 'pegal' atau
rasa tidak nyaman di daerah lesi. Selanjutnya
jika terjadi penekanan pada radiks akan
muncul nyeri radikular yang menjalar dari
punggung sesuai dengan daerah radiks yang
terkena. Pada nyeri di daerah torakal, nyeri
seperti terikat atau keram ke perut yang
sering disalah artikan oleh pasien ataupun
klinisi lain sebagai nyeri abdomen. Pada
pemeriksaan fisik biasanya akan ditemukan
nyeri tekan yang menunjukkan adanya
komponen nyeri nosiseptif bersamaan
dengan nyeri neuropatik.
Nyeri sontak harus dapat dibedakan dengan
eksaserbasi rasa nyeri sebagai akibat dari
kegagalan dosis terapi analgesia sesuai
dengan waktu paruh obat ini dalam
tubuh. Untuk membedakannya, dapat
dilakukan pencatatan rasa nyeri (buku harlan
nyeri) untuk menentukan bahwa pola yang
terjadi yaitu akibat kegagalan dosis terapi
analgesia terkait jadwal pemberian, sehingga
diperlukan modifikasi pemberian jadwal.
Diagnosa
Seperti halnya penyakit lain, Diagnosa
nyeri kanker ditegakkan melalui anamnesis,
pemeriksaan fisik, dan penunjang untuk
mendapatkan karakteristik nyeri dan
konfirmasi Diagnosa nyeri kanker. Untuk
lebih memudahkan tata laksana, data
karakteristik nyeri dan temuan fisik
yang merupakan konsekuensi spesifik
dari penyakit kanker atau terapinya
dikumpulkan ke dalam suatu sindrom, yaitu
sindrom nyeri kanker.
Sindrom nyeri kanker dapat digolongkan ke
dalam akut dan kronik (Tabel 2). Sindrom
nyeri kanker akut biasanya berhubungan
dengan intervensi diagnostik atau terapeutik,
sedangkan kronik biasanya disebabkan oleh
perkembangan tumor secara langsung
Menurut International Association for the
Study of Pain (IASP), suatu nyeri dapat
dikatakan nyeri kronik jika dirasakan ada
nyeri yang melewati batas waktu normal
dari fase penyembuhan jaringan, bisa lebih
dari 3 atau 6 bulan. Pada nyeri kanker,
lebih dari 3 bulan ditentukan sebagai
nyeri kronik. Pada kenyataannya, banyak
sindrom nyeri kanker dikategorikan sebagai
kronik walaupun belum melewati fase
penyembuhan jaringan.
PENGOBATAN
PENGOBATAN nyeri kanker berdasar WHO
diawali dengan penilaian aspek penyakit
kanker itu sendiri dan aspek nyeri yang
dirasakan oleh pasien. Dengan kedua jenis
penilaianini, dapatdiidentifikasi karakteristik
dan etiologi nyeri yang dihubungkan dengan
kondisi penyakit kankernya. Proses ini
berlanjut dengan penentuan target yang
realistis dan modalitas terapi nyeri yang
akan diimplementasikan pada pasien, yaitu:
1. Terapi simtomatis dan suportif: berupa analgesik beserta adjuvannya, terapi nonfarmakologis (psikososial dan spiritual) atau
radioterapi.
2. Terapi definitif, dengan menghilangkan
dan mengecilkan ukuran massa tumor
sebagai sumber nyeri; terutama berupa
reseksi tumor, atau memakai
kemoterapi dan radioterapi.
Pada prinsipnya, proses PENGOBATAN nyeri
secara umum terdiri dari 5 tahapan utama,
yaitu penilaian (assessment), Analisa karakteristik nyeri, terapi, evaluasi terapi, dan
dokumentasi. Setiap tahapan dibuat berkesinambungan dan berulang-ulang sesuai
kondisi pasien. Dengan demikian, bila se-
648
tiap kali pasien mengeluhkan nyeri, maka
kelima proses ini harus dijalankan secara
berurutan.
1. Penilaian Nyeri
Walaupun prevalensinya tinggi, tidak
semua pasien· mengakui dalam keadaan
nyeri. Hal ini dapat disebabkan oleh karena
pasien merasa wajar penderita kanker
mengalami nyeri, atau karena pasien
takut mendapat penambahan obat-obatan
disamping obat-obat utama yang sudah
diterimanya. Jadi nyeri harus ditanyakan
secara khusus atau diperkirakan dari
besarnya massa, adanya daerah yang
ulkus, atau pada pemeriksaan penunjang
tampak gambaran kerusakan tulang atau
jaringan saraf di sekitarnya. Demikian pula
pada pasien dengan penurunan kesadaran,
nyeri dapat berupa menyeringai di wajah
atau gelisah.
2. Analisa Nyeri
a. Derajat beratnya nyeri: ditentukan
termasuk nyeri ringan, sedang,
atau berat Skala yang paling umum
dipakai yaitu Visual Analog Scale
(VAS) atau Numeric Rating Scale
(NRS) untuk pasien yang sadar dan
kooperatif. Secara kuantitatif, skala
nyeri berdasar NRS dari 0 (tidak
nyeri) hingga 10 (sangat nyeri). Nyeri
dinyatakan sebagai nyeri ringan jika
memiliki nilai NRS 1-3, nyeri sedang
(NRS 4-6), dan nyeri berat (7-10).
Pada pasien yang tidak kooperatif atau
tidak sadar dapat dipakai Face, Legs
Activity, Cry, Conso/abi/ity (FLACC) Scale.
b. Tipe nyeri: nyeri neuropatik, nosiseptif,
atau nyeri campuran (mixed pain).
c. Durasi: akut, kroninyek, atau nyeri
sontak
d. Lokasi: lokal, atau radikular (jika
menjalar sesuai dengan persarafan dari
sumber nyeri ke area lain)
3. Evaluasi
Pasien yangtelah ditentukan targetterapi
dan mendapatkan terapi nyeri harus
dievaluasi dan dipantau keberhasilannya.
Evaluasi ini tergantung derajat nyerinya;
pada nyeri ringan dipantau setiap 8 jam,
nyeri sedang setiap 2 jam, dan nyeri
berat setiap 1 jam. Targetnya yaitu
pengurangan nyeri hingga 30% dan
perbaikan fungsional. Jika nyeri belum
berkurang atau muncul nyeri baru, maka
harus dilakukan penilaian ulang dengan
proses yang sama seperti sebelumnya.
4. Terapi
Pemberian terapi simptomatis nyeri
dengan memakai WHO stepladder
(Gambar 4) mengacu kepada skala nyeri:
nyeri ringan pada anak tangga pertama,
nyeri sedang merupakan anak tangga
kedua, dan nyeri berat menempati anak
tangga ketiga. Setiap anaktangga memiliki
golongan obat simptomatis nyeri masingmasing. Contoh penerapannya, hila
pasien tergolong nyeri ringan, maka
golongan obat nyeri yang diberikan
yaitu analgesik non-opioid dengan
atau tanpa adjuvan. Jika pasien masih
mengeluh nyeri walaupun telah diberikan
golongan obat pada anak tangga ketiga
maka pasien direncanakan mendapat tata
laksana intervensi nyeri, antara lain blok
saraf (somatik, simpatetik), medikasi dan
stimulator spinal, serta pembedahan.
Studi menunjukkan terapi farmakologis
dengan kerangka kerja seperti ini relatif
649
Nyeri Kanker
tidak mahal dan 70-90% efektif.
5. Dokumentasi
Kesemua proses harus didokumentasikan agar memudahkan proses evaluasi,
terutama jika nyeri sulit ditangani atau
adanya nyeri sontak yang dosis obatnya
dihitung berdasar dosis harlan, serta
pada titrasi opioid dari parenteral ke oral.
PENGOBATAN ini juga harus masuk
dalam 5 prinsip PENGOBATAN nyeri WHO,
yaitu:
1. Sesuai jalur mulut
Administrasi obat secara oral nyaman,
non-invasif, dan dapat ditoleransi dengan baik
2. Sesuai jam pemberian obat
Analgesik yang diperlukan ditaruh
berdasar waktu paruh obat, diperlukan untuk menjaga kadar terapeutik
obat tetap konstan dalam darah.
3. Sesuai WHO stepladder
4. Sesuai individu
Dikhususkan dengan karakteristik masing-masing pasien, indikasi, kontraindikasi, alergi, dosis koreksi gagal ginjal,
dan sebagainya.
5. Sesuai perhatian terhadap detil
Dokumentasi nilai skala nyeri yang
tercatat baik, total obat harus dijumlahkan dalam 24 jam, memperhatikan
keluhan nyeri dasar, nyeri dasar terkontrol dan nyeri sontak
Konsep PENGOBATAN nyeri kanker berdasar
WHO stepladder memiliki beberapa prinsip,
yaitu:
• Analgesik harus diberikan secara teratur
dengan dosis adekuat untuk menjaga
level terapeutik obat dalam darah.
• Analgesik dapat dieskalasi secara berurutan
sesuai tingkatan tangga WHO stepladder.
• Di samping pemberian obat regular,
pasien harus mendapat pengobatan
untuk nyeri sontak.
• Efek samping anagesik, terutama
konstipasi dan mual, harus diantisipasi
dan diberikan pencegahan pacta pasien.
• Pemantauan secara teratur dan cermat
penting dilakukan pacta pasien yang
mendapat analgesik
• Pasien harus mendapat akses yang mudah
untuk memperoleh analgesik saat kapanpun mengalami nyeri.
berdasar WHO stepladder, ada dua
jenis analgesik, yaitu opioid dan non-opioid.
Pemberian jenis analgesik ini tergantung
intensitas nyeri pasien. Nyeri dengan intensitas ringan dapat diberikan analgesik
non-opioid, misalnya golongan obat antiinflamasi nonsteroid (OAINS), dengan dosis
sesuai Tabel 3.
Ada pun nyeri dengan intensitas sedangjberat
diberikan analgesik opioid (Tabel 4). Pacta
pasien dengan intensitas ini, pemakaian
OAINS intravena tetap ada indikasinya,
misalnya pacta kondisi akut/ emergensi dalam
jangka waktu pendek atau nyeri nosiseptif
dengan keterlibatan muskuloskeletal dan
jaringan lunak. Oleh sebab itu, pemberian
analgesik pacta nyeri kanker tidak bersifat
kaku, melainkan individual sesuai kondisi
patologis yang terjadi
NCCN 2016 membedakan pasien pengguna
opioid baru ( opioid-naive) dan pasien
pengguna opioid rutin (opioid-tolerant).
Definisi pengguna opioid baru yaitu
pasien yang tak pernah memakai
opioid secara kronik atau pengguna opioid
dengan jumlah dosis opioid harian kurang
dari ambang batas dosis opioid pengguna
opioid rutin dan pemakaian dosis ini
kqrang dari 1 minggu.
Adapun pengguna opioid rutin yaitu pasien
yang rutin memakai opiod dalam
semingguataulebihdengan jumlahdosisharian
melebihi atau sesuai dengan dosis ambang
batas, antara lain morfin 60mgfhari oral,
fentanil transdermal 251lg/jam, hidromorfon
651.
8mg/hari oral, oksimorfon 25mgfhari oral,
atau opioid lain yang setara (TabelS).
Sebagai contoh, pasien yang telah mendapat
dosis morfin 70mgfhari dengan pemakaian
lebih dari 1 minggu dapat dikatakan sebagai
pengguna opioid rutin. Pasien dengan
dosis morfin 40 mg/hari selama kurang
dari 1 minggu disebut pengguna opioid
baru. Sementara itu pada kasus lain, pasien
pengguna morfin 40mg/hari lebih dari 1
minggu dapat termasuk pengguna opioid
rutin menurut panduan NCCN 2010. ·
PENGOBATAN nyeri kanker pada pasien
pengguna opioid baru selanjutnya dibagi
berdasar intensitas nyeri. Semakin tinggi
skala nyeri, semakin dianjurkan untuk segera
titrasi opioid. Namun, ada beberapa hal yang
harus diperhatikan secara umum untuk
semua tingkat intensitas nyeri, antara lain:
• pemakaian opioid sesuai prinsip,
dengan titrasi, dan kontinu
• Antisipasi efek sam ping analgesik
• Pemberian dukungan psikososial
• Edukasi pasien dan keluargafperawat
• Optimatisasi intervensi yang bersifat
integratif
• Pertimbangan pemakaian NSAID atau
asetaminofen
• Untuk nyeri yang akut dan intensitas
berat, segera datang ke RS
Berbeda dengan pengguna opioid baru, tata
laksana nyeri kanker untuk pengguna opioid
rutin dapat memakai opioid oral atau
intravena. Pemberian opioid oral memiliki
efek puncak dalam 60 menit. Di lain pihak,
pemberian opioid intravena memiliki efek
puncak dalam 15 menit. Dosis opioid yang
diberikan, baik oral maupun intravena,
sebesar 10-20% dari total dosis opioid yang
diterima selama 24 jam terakhir.
Selanjutnya pasien dievaluasi efikasi dan efek
sampingyang dirasakan sesuai efekpuncaknya,
yaitu 15 menit (intravena) dan 60 menit (oral).
Bila nyeri tidak berkurang atau bertambah
berat, maka dosis opioid dinaikkan 50-100%.
Bila nyeri berkurang namun belum sepenuhnya
terkontrol, maka opioid dapat diberikan ulang
dengan dosis yang sama dengan sebelumnya.
Kedua hal ini harus dievaluasi lagi dan dapat
diulang hingga 2-3 siklus. Bila kemudian
nyerinya belum terkontrol, maka klinisi harus
evaluasi ulang dari awal mengenai nyeri
(reassessment) secara komprehensif dan
melakukan penanganan secara integratif. Bila
nyerinya sudah terkontrol, maka dosis opioid
terkini dilanjutkan sebagai dosis efektif untuk
652
pasien ini
Pemberian opioid pada pasien nyeri kanker
harus memperhatikan efek sampingnya
juga, karena sering terjadi dan harus dapat
diantisipasi serta ditangani secara agresif
(Tabel 6). Mengingat banyaknya pengobatan
yang didapat oleh pasien kanker, maka setiap
efek samping opioid yang terjadi harus pula
dipikirkan pemicu selain opioid. Oleh
sebab itu, perlu penilaian secara multisistem.
Penggantian Opioid ( Opioid Switching)
Adakalanya terdapatkondisi perlu dilakukan
penggantian opioid (opioid switching), yaitu
proses penggantian suatu opioid ke opioid
lain untuk mendapatkan efek antinyeri
lebih baik dengan efek samping seminimal
mungkin. Proses penggantian ini bersifat
individual bergantung respons pasien
dengan penilaian yang komprehensif.
Parameter keberhasilannya yaitu jika
terjadi penurunan intensitas nyeri <::33%
danfatau berkurangnya efek samping
terkait opioid.
Indikasi penggantian opioid antara lain
nyeri yang terkontrol namun muncul efek
samping serius, nyeri belum terkontrol
adekuat namun tidak bisa ekskalasi dosis
opioid karena efek sam ping, atau nyeri yang
belum terkontrol dengan opioid walaupun
tanpa efek sam ping.
Langkah-langkah penggantian opioid yaitu
sebagai berikut:
1. Hitungtotal dosis harlan opioid pasien terkini.
2. Estimasi total dosis opioid yang ingin
dipakai dengan konversi opioid memakai tabel ekuivalensi (Tabel 7 dan
8). Tabel ini memakai morfin oral sebagai
acuan, sehingga konversi dosis opioid
lainnya harus diubah ke morfin dahulu,
kemudian baru ke jenis opioid yang dikehendaki. Misalnya, penggantian kodein ke
oksikodon dilakukan dengan cara mengkonversi kodein ke morfin, kemudian marfin ke oksikodon.
3. Turunkan total dosis estimasi ini
sebesar 50% (jika pasien dalam dosis
tinggi opioid) atau 25-40% (jika pasien
dalam dosis opioid rendahjsedang).
4. Sesuaikan dosis tergantung kondisi
individual pasien, misalnya:
• Tipe nyeri akut atau kronik; dosis
lebih tinggi pada nyeri akut.
• Disfungsi hepar jhati; penyesuaian
dosis diperlukan pada gangguan
kedua organ ini .
• Usia; mulai dengan dosis rendah pada
pasien usia lanjut karena lebih rentan
mengalami efek sam ping.
• Medikasi; pasien dengan polifarmasi
mungkin perlu penyesuaian dosis
untuk mencegah efek sam ping akibat
interaksi obat.
5. Dosis estimasi yang telah disesuaikan
ini kemudian diberikan secara
titrasi naik, hingga dapat mengontrol
nyeri. Opioid lepas cepat (immediate
release) bisa diberikan untuk nyeri
sontak, terutama saat masa titrasi
dengan dosis sebesar 10-15% dari total
dosis harian.
6. Anjurkan kepada pasienfpengasuhnya
untuk mencatat tanda dan gejala nyeri
yang belum terkontrol, termasuk jumlah
dosis untuk nyeri sontak. Selain itu, efek
samping sedasi juga perlu didokumentasikan.
7. Pantau ulang pasien untuk menilai
kontrol nyeri dan efek samping obat.
Hal ini dapat dilakukan 3 hari setelah
memulai opioid baru, atau waktu lain
sesuai kondisi pasien.
8. Perubahan opioid dari rute intravenake oral
harus dalam pemantauan dokter, pasien
harus berada dalam perawatan setidaknya
pada 24 jam pertama perubahan.
Kombinasi Obat
Di sam ping opioid, PENGOBATAN nyeri kanker
juga melibatkan adjuvan analgesik yang
bertujuan untuk menurunkan kebutuhan opioid, sehingga efek sampingnya dapat
berkurang. Antidepresan dan antikonvulsan
yaitu lini pertama adjuvan analgesik
(Tabel 9). Obat-obatan ini dapat membantu
pasien nyeri kanker yang belum sepenuhnya
terkontrol dengan opioid. Oleh karena
respons yang bervariasi, maka pemilihan
jenis obatnya dapat mempertimbangkan
kondisi dan komorbiditas pasien. Misalnya
adjuvan analgesik yang berefek sedasi bisa
bermanfaat untuk pasien yang insomnia,
atau yang mengalami kecemasan dapat
diberikan amitriptilin. Amitriptilin juga
berguna pada nyeri kronik yang dapat
merupakan kelanjutan dari nyeri kanker jika
lama belum mendapatkan terapi definitif.
Pada pasien dengan nyeri kanker biasanya
akan ada komponen nyeri kanker
akibat infiltrasi sel tumor ke sera but saraf di
sekitarnya. Namun hal ini sering terabaikan
oleh klinisi, padahal terapi yang tepat akan
sangat membantu pasien. Oleh karena itu
diperlukan adjuvan golongan antikonvulsan
yang dosis antikonvulsan selengkapnya
dapat dilihat pada bab Nyeri Neuropatik.
Darl kesemua antikonvulsan, kombinasi
gabapentin dan opioid menunjukkan
adanya penambahan kekuatan dan kerja
sinergis, sehingga efektif dalam dosis
opioid yang lebih kecil secara signifikan
dibandingkan opioid saja. Hal ini terutama
pada karakteristik nyeri panas atau seperti
ditusuk-tusuk yang tidak terlalu berkurang
dengan hanya opioid. Demikian pula
kombinasi ini dapat mengurangi efek
sam ping opioid, seperti konstipasi dan mual
secara bermakna. Dosis gabapentin dapat
dimulai dari 300mgfhari naik perlahan
hingga maksimal 3600mg.
Opioid juga dapat dikombinasi dengan OAINS,
terutama jika komponen nyerl nosiseptif yang
dominan, yang ditandai dengan pembesaran
massa tumor hingga memicu kerusakan
jarlngan. Parasetamol paling serlng dikombinasi, baik dengan hidrokodon (kodein sintetik), oksikodon, maupun tramadol. Kombinasi
paracetamol dengan hidrokodon dapat menurunkan nyerl lebih dari 50% dengan dosis awal
2500mg-25mg/24 jam. Dosis dapat ditingkatkan hingga dosis maksimal4000mg-50mg/24
jam. Kombinasi parasetamol-tramadol dapat
dilakukan sebagai salah satu pemberian terapi nyerl sontak sebagai adjuvan dengan dosis
awal 325mg-37,5mg perkali jika pemakaian
dosis harlan tramadol s400mg atau dosis harlan kodein s300mg atau dosis harlan morfin
<60mg. Jika dosis harlan morfin 60-120mgf24
jam maka pemberian dapat diberikan 2 tablet
kombinasi parasetamol-tramadol. Tramadol
sendirl dapat sebagai terapi ajuvan pemberlan pada dosis awal tramadol 200mgfhari
dapat menghilangkan keluhan nyerl sebanyak
60% dan dapat diberlkan hingga dosis maksimal400mgfharl.
656
Adjuvan analgesik nyeri kanker dapat
berupa obat topikal (lidokain patch 5%)
dan kortikosteroid. Deksametason lebih
dipilih karena efek mineralokortikoid yang
lebih minimal. pemakaian kortikosteroid
ini terutama bermanfaat pada nyeri akut
yang melibatkan struktur saraf dan tulang.
Hindari kombinasi tramadol dengan amitriptilin atau karbamazepin dapat memicu kondisi renjatan (shock) akibat sindrom serotonin.
Nyeri kanker dapat dikatakan telah
terkontrol jika setelah mendapat tata
laksana, nyeri dirasakan hilang atau
berkurang 50%, dan dapat ditoleransi pada
keadaan tertentu. Konsep nyeri terkontrol
ini disampaikan dengan pengertian yang
sesuai dengan harapan dan pendidikan
pasien.
Patokan kesuksesan terapi yang sesuai dan
secara bertahap yaitu :
• Rasa nyeri terkontrol pada saat tidur
malam
• Rasa nyeri terkontrol pada saat istirahat
dalam sehari penuh
• Rasa nyeri terkontrol pada saat mobilitas
terbatas
• Rasa nyeri terkontrol pada saat mobilitas
penuh
Terapi Definitif dan Suportif
Pada nyeri yang diakibatkan oleh ukuran
massa yang besar, perlu dilakukan reseksi
atau pengurangan volume tumor untuk
mengurangi nyeri dengan tindakan operatif,
kemoterapi, atau radioterapi. Radioterapi
juga berperan pada nyeri akibat metastasis
ke tulang vertebra, dengan menginaktivasi
sel tumor mencegah proses kerusakan lebih
lanjut. Demikian pula pemberian bifosfonat,
suatu agen penghambat osteoklas akan
berperan menurunkan resorpsi tulang yang
memicu nyeri. Kesemua hal ini
akan sangat membantu mengurangi dosis
obat-obatan terutama opioid, sehingga
pasien juga bisa terhindar dari efek sam ping
yang berlebihan.
CONTOH KASUS
Seorang laki-laki 52 tahun datang dengan
keluhan utama nyeri leher yang menjalar
Nyeri Kanker
ke belakang kepala sejak 3 hari lalu. Keluhan dimulai sejak 5 bulan sebelumnya,
ada benjolan di leher kiri. Benjolan ini disertai nyeri yang semakin
memberat, hingga sebulan yang lalu dibiopsi dengan hasil karsinoma nasofaring
(KNF). Lalu pasien menjalani kemoterapi.
Nyeri dirasakan menjalar dari daerah
benjolan ke leher belakang yang semakin memberat (NRS=7 -8) dan membuat
pasien sulit tidur.
Pemeriksaan fisik neurologis tidak didapatkan defisit. Status lokalis di regio colli dekstra teraba massa ukuran Sx4x2 em dengan
nyeri tekan, konsistensi keras, tidak dapat
digerakkan (Gambar 5).
Hasil CT scan nasofaring menunjukkan massa di nasofaring sisi kiri yang mengobliterasi fossa Rossenmuller dan torus tubarius
kiri, mengisi koana kiri, orofaring, spasium
parafaring kiri, mengobliterasi M. Pterigoid
medialis kiri, disertai limfadenopati multipel regio colli bilateral (Gambar 6).
Pertanyaan
1. Bagaimana karakteristik nyeri pasien?
a. Nyeri nosiseptif ·
b. Campuran nyeri· neuropatik dan
nosiseptif
c. Akut
d. Bersifat radikular
e. Intensitas ringan sedang
Jawaban: (B) ada lesi benjolan
dengan tanda inflamasi dan adanya
nyeri tekan yang menunjukkan nyeri
nosiseptif, disertai rasa nyeri menjalar
yang berarti nyeri neuropatik.
2. Apakah pemicu nyeri pada keluhan
utama pasien?
a. Peradangan lokal
b. Kerusakan jaringan pada kanker
, c. Psikogenik
d: Infiltrasi sel tumor ke serabut saraf
, e. ,_spasme otot
•.. Jawaban: TD); wa,Iauptin memang ada
kerusakan jaringan yang memicu
658
nyeri, namun keluhan utama pasien
ini yaitu nyeri yang menjalar yang
menunjukkan adanya infiltrasi sel tumor
ke serabut saraf, dalam hal ini radiks
daerah servikal.
3. Apakah analgesik adjuvan pilihan utama
yang sebaiknya diberikan pada pasien?
a. Diazepam
b. Pregabalin
c. Amitriptilin
d. Asam valproat
e. Gabapentin
Jawaban: (E); pemilihan adjuvan disesuaikan dengan kondisi pasien. Adanya nyeri
neuropatik memicu adjuvan diprioritaskan golongan antikonvulsan. Dari
semua golongan antikonvulsan, yang
dapat meningkatkan potensiasi analgesik
dari opioid yaitu gabapentin. Jika pasien
ada kecemasan dapat diberikan
amitriptilin, namun obat ini tidak dapat
dikombinasi dengan tramadol, jika memang direncanakan pemberian tramadol
selanjutnya pada pasien.
4. Bagaimana PENGOBATAN etiologi nyeri
pada pasien ini?
a. Antiinflamasi nonsteroid
b. Akuptintur
c. Kemoradiasi
d. Radioterapi
e. Hipnosis . .
Jawaban: (C); nyeri akibat perluasan
massa tumor harus dikecilkan ukurannya
sesuai dengan jenis tUmor. ·Pada KNF
terapi utama yaitu kemoterapi dan/
atau radioterapi.
5. Apakah PENGOBATAN awal untuk
mengatasi nyeri pasien ini?
a. Ketorolak 30mg IV
b. Parasetamol 500mg PO
c. Midazolam 5mg IV
d. Kodein 20mg PO
e. Gabapentin 100mg PO
Jawaban: (A); pasien ini mengalami nyeri
derajat sedang berat yang mengganggu,
sehingga perlu pemberian anti nyeri
dengan jalur intravena. Adanya tandatanda kerusakan jaringan menunjukkan
nyeri nosiseptif, sehingga dapat diberikan go Iongan OAINS seperti ketorolak IV.
Lanjutan Kasus
Pasien mendapat PENGOBATAN awal ketorolak 30 mg/8 jam IV karena dianggap nyeri
akut yang sudah mengganggu aktivitas, NRS
turun menjadi 4-5. Nyeri masih terasa terutama menjalar, maka dianggap sebagai nyeri
neuropatik, sehingga diberikan gabapentin
600mgjhari. Oleh karena ketorolak tidak
boleh diberikan lebih dari 5 hari, maka diganti menjadi tramadol dosis awal 100mg/
hari, titrasi naik NRS pasien turun menjadi
2-3. Pasien lalu menjalani kemoradiasi untuk
mengatasi etiologi nyerinya, dan NRS turun
lagi menjadi 1-2. Tramadol turun bertahap
diganti paracetamol2000mgjhari, gabapentin dosis 300mgjhari. Selanjutnya bisa dipakai kombinasi paracetamol dan tramadol
dosis rendah sebagai rumatan, beserta gabapentin jika nyeri masih terasa menjalar.
NEUROPATI
Sistem saraf perifer terdiri dari saraf-saraf
kranial (kecuali nervus olfaktorius dan
optikus), saraf-sarafyang berasal dari medula
spinalis (radiks, rami, trunkus, pleksus,
maupun saraf perifer itu sendiri, seperti
saraf medianus dan tibialis), dan komponenkomponen dari sistem saraf otonom di perifer.
Bah ini akan menjelaskan tentang gangguan
pada sistem saraf perifer atau yang secara
umum dapat dikelompokkan dalam satu
entitas, yaitu neuropati.
EPIDEMIOLOGI
Prevalensi neuropati bervariasi an tara 2-85%,
tergantung dari prevalensi etiologi pemicu nya. Di RSUPN Cipto Mangunkusumo Jakarta
tahun 2012-2014, angka kejadian neuropati
yang diinduksi kemoterapi pada pasien
karsinoma nasofaring sebesar 76%, sedangkan sindrom terowongan karpal diperkirakan
terjadi pada 3,8% dari populasi umum, dengan
insidens 276 per 100.000 populasi.
663
PATOFISIOLOGI
Patofisiologi neuropati beragam tergantung
dari etiologinya, yaitu genetik, metabolik, dimediasi imunitas, infeksi, toksik, traumatik,
dan lain-lain. Namun hal ini akan lebih mudah
dipahami secara umum dengan mengetahui
kerusakan sera but sarafberdasar anatomihistologinya.
Neuropati dapat terjadi karena lesi di badan
sel saraf ( neuronopati) maupun pada akson
di serabut saraf perifer (neuropati perifer).
Neuronopati dapat terjadi karena kerusakan
pada badan sel saraf di kornu anterior, atau
sering dikenal dengan motor neuron disease.
Neuronopati juga dapat terjadi karena
kerusakan pada ganglion radiks dorsalis
tern pat badan sel saraf sensorik orde I, yang
dikenal sebagai neuronopati sensorik atau
ganglionopati. Adapun neuropati perifer
terjadi karena kerusakan pada akson atau
mielin di serabut saraf perifer. Oleh karen a itu
neuropati perifer dapat dibagi menjadi dua
kategori, yaitu aksonopati dan mielinopati
(Gambar 1)
Apabila terjadi kerusakan akson, secara
teori akan terjadi hambatan hantaran
impuls saraf baik eferen maupun aferen.
Kerusakan pada selubung mielin juga dapat
memicu hambatan impuls saraf. Impuls
saraf yang dihantarkan akson bermielin
akan dikonduksikan lebih cepat dengan cara
saltatory conduction (konduksi lompatan).
Hal ini terjadi karena selubung mielin akson
bertindak sebagai isolator; sehingga konduksi
listrik melompat dari satu nodus Ranvier ke
nodus berikutnya. Apabila terjadi kerusakan
selubung mielin saraf, maka kecepatan
koduksi impuls saraf akan jauh menurun
atau bahkan terhenti. Patofisiologi kerusakan
ini dapat di-nilai secara klinis dengan bantuan
pemeriksaan kecepatan hantar saraf (KHS),
seperti pada Tabell. Pemeriksaan konduksi
han tar saraf akan menilai amplituda, termasuk
dispersi temporal (lihat Bab Sindrom GuillainBarre tentang KHS), yang menggambarkan
seberapa banyak serabut saraf teraktifasi dan
kecepatan hantar saraf (velocity) mulai dari
titik stimulasi sampai tern pat perekaman.
Lesi di badan sel saraf dan akson akan diikuti oleh proses degenerasi serabut akson
yang berada di distal dari lesi, yang disebut
sebagai degenerasi Wallerian. Degenerasi ini
terjadi karena pengaturan metabolisme sel
saraf berada di badan sel. Pengaturan metabolisme terse but diteruskan ke akson yang
lebih distal melalui suatu mekanisme yang
disebut sebagai axonal transport dan terjadi
secara anterograd dan retrograd. Apabila
hubungan antara badan sel dengan akson
distal terputus akibat kerusakan akson di
antara keduanya maka axonal transporttidak
dapat terjadi, sehingga akson bagian distal
tidak dapat mempertahankan metabolismenya dan mengalami degenerasi.
665
Neuropati
Neuropati juga dapat dibagi berdasar
diameter akson yang mengalami kerusakan,
yaitu:
a. Akson berdiameter besar-bermielin;
di antaranya akson untuk serabut motorik (alpha motor neuron) dan sensorik
untuk menghantarkan stimulus propioseptif, vibrasi, dan sentuhan ringan.
b. Akson berdiameter kecil-bermielin;
termasuk serabut sensorik yang menghantarkan stimulus sentuhan ringan,
nyeri, suhu, dan serabut saraf otonom
preganglion.
c. Akson berdiameter kecil-tidak bermielin; membawa stimulus nyeri, suhu,
dan sera but saraf otonom pascaganglion.
GEJALA DAN TANDA KLINIS
Gejala neuropati cukup beragam, mulai dari
gejala motorik, sensorik, maupun otonom.
Gejala ini dapat sama, walaupun akibat etiolologi yang berbeda. Untuk mempermudah menegakkan Diagnosa , gejala klinis
ini dibagi menjadi gejala positif dan negatif,
baik motorik maupun sensorik Gejala positif motorik dapat berupa aktivitas abnormal
berlebih dari neuron, di antaranya kekakuan,
twitching, dan miokimia. Gejala positif sensorik diantaranya rasa terbakar, tersayat,
alodinia atau hiperalgesia, dan parastesia.
Adapun gejala negatif motorik mencerminkan berkurangnya aktivitas neuron, misalnya
berkurangnya kekuatan motorik, kelelahan,
atrofi otot. Gejala negatif sensorik biasanya
hipestesia serta gangguan input informasi
dari luar tubuh lainnya, seperti gangguan
input posisi tubuh, sehingga terjadi ataksia
dan gangguan keseimbangan.
Gejala otonom dapat berupa konstipasi, diare, impotensi, inkontinesia uri, gangguan
berkeringat karena gangguan vasomotor,
dan pusing yang berkaitan dengan perubahan posisi ( ortostasis ). Pasien yang mengalami
gangguan vasomotor biasanya mengeluhkan
telapak tangan atau kaki dingin disertai perubahan warna kulit. Gangguan vasomotor ini
disebabkan karena pembuluh darah di kulit
mengalami gangguan refleks untuk vasokonstriksi dan vasodilatasi yang diatur oleh saraf
otonom dalam menghadapi perubahan suhu
tubuh.
Anamnesis aktivitas sehari-hari seperti perubahan tulisan tangan, kesulitan mengancingkan baju, kesulitan memakai sendal
jepit karena sering terlepas sangat berguna
dalam menegakkan Diagnosa . Pertanyaan
terperinci tentang onset, durasi, dan progresifitas defisit neurologis yang ada juga
sangat penting untuk membedakan jenis
neuropati. Perlu ditanyakan juga kepada
pasien ten tang keasimetrisan dan distribusi
gejala klinis saat onset, keterlibatan batang
tubuh atau nervus kranial, dan laju progresifitasnya secara spesifik (monofasik, berfluktuasi, atau berjenjang). Selanjutnya anamnesis
ini dikonfirmasi dengan pemeriksaan
fisik untuk mencari distribusi defisit neurologis, yang dibagi menjadi defisit fokal, multifokal, ataupun distal simetrik.
Pemeriksaan fisik sensorik dapat dibagi dua
berdasar jenis serabut saraf sensorik
yang dinilai. Pemeriksaan untuk serabut
saraf besar yaitu tes vibrasi, posisi sendi
(propioseptif), dan raba hal us, termasuk tes
Romberg, sedangkan untuk serabut saraf
kecil dilakukan pemeriksaan tes cukit kulit
dan suhu. Sesungguhnya pemeriksaan raba
666
hal us yaitu memeriksa batas bawah reseptor mekanik (mechanoreceptor low threshold) yang dihantarkan oleh kedua serabut
saraf baik besar dan kecil. Pemeriksaan
fungsi serabut saraf kecil yang menghantarkan rasa nyeri dapat dilakukan dengan menyentuhkan benda berujung tajam seperti
tusuk gigi tanpa tekanan yang signifikan.
Saat melakukan pemeriksaan fungsi saraf
sensorik, harus sudah dipikirkan pola
parastesifanestesi berdasar sebaran
anatominya, lebih sesuai untuk mononeuropati, polineuropati distal simetrik, lengthdependent polineuropathy, polineuropati
mutifokal, radikulopati, pleksopati, atau
kemungkinan adanya keterlibatan sistem
saraf pusat (SSP).
Pemeriksaan motorik dimulai dari inspeksi
ada tidaknya atrofi maupun fasikulasi. Palpasi dilakukan untuk menilai tonus dan
rigiditas otot untuk menyingkirkan diagnosis banding gangguan SSP. Pemeriksaan
kekuatan motorik pada neuropati perlu
dilakukan secara spesifik, terperinci sesuai
dengan otot dan saraf perifer yang terganggu.
Misalkan pada neuropati nervus medianus
di pergelangan tangan, otot-otot intrinsik
tangan yang dipersarafi oleh N. Medianus
(M. Aduktor Polis is Brevis) harus diperiksa
kekuatannya. Namun otot-otot intrinsik
tangan lain yang tidak dipersarafi oleh N.
Median us, seperti M. Interosesus Digiti I dan
M. Abduktor Digiti Minimi oleh N. Ulnaris
perlu juga diperiksa untuk menyingkirkan
Diagnosa banding neuropati pada N. Ulnaris. Pemeriksaan ini perlu dilakukan pada
seluruh ekstremitas, khususnya bila neuropati yang dicurigai yaitu polineuropati.
Pemeriksaan saraf otonom harus dilaku
kan, karena akan memberi informasi lebih
banyak mengenai Diagnosa banding, etiologi,
maupun sindrom pada pasien. Gangguan ortostatik dapat memberi petunjuk bahwa
sudah terjadi gangguan otonom karena
gangguan saraf otonom dapat memicu gangguan vasokonstriksi dan vasodilatasi pada pembuluh darah. Pemeriksaan
saraf otonom juga dapat dilakukan dengan
memeriksa kulit dan membran mukosa
karena gangguan saraf otonom dapat memicu gangguan vasomotor pada kulit.
Di sisi lain, pemeriksaan kulit yang terkait
mapupun yang tidak terkait otonom dapat
membantu menyingkirkan Diagnosa banding.
Gambaran ruam vaskulitis (purpura, livedo
retikularis ), hiperpigmentasi bila disertai
dengan polineuropati, organomegali, endokrinopati dapat membantu menegakan
Diagnosa sindrom (POEM) polineuropati,
pulmonary disease, organomegali, edema,
endokrinopati, monoklonal paraprotein. Jika
ada ulkus pada rongga mulut maka dapat
dipikirkan adanya neuropati pada penyakit
Behcet atau HIV. Mata dan mulut kering, pembengkakan kelenjar saliva dapat ditemui pada
sarkoidosis atau sindrom Sjogren.
Diagnosa KLINIS DAN Diagnosa
BANDING
Neuropati secara klinis dapat dibagi menjadi polineuropati, neuropati fokal, dan multifokal. Polineuropati disebabkan oleh agenagen yang bekerja secara difus terhadap
sistem saraf perifer seperti bahan beracun
(toksik), defisiensi zat-zat yang diperlukan
dalam metabolisme saraf perifer, gangguan
metabolik, dan beberapa reaksi imun. Adapun lesi fokal (mononeuropati) dan lesi
multifokal yang terisolasi (multipel mono-
667
Neuropati
neuropati atau mononeuropati multipleks)
disebabkan oleh kerusakan lokal di antaranya penjepitan saraf seperti carpal tunnel
syndrome (CTS), cedera mekanik (karena
tekanan, traksi, ledakan, dan penetrasi),
suhu ekstrim (panas maupun dingin), elektrik, radiasi, lesi vaskuler, granulomatosa, keganasan atau proses infiltratif lainnya, dan
tumor primer saraf perifer.
Di Indonesia, salah satu pemicu tersering
mononeuropati multipleks yaitu kusta.
Gejala yang sering muncul pada neuropati
kusta yaitu gangguan sensorik berupa
anestesi atau gangguan peraba terutama di
distal jari-jari termasuk ibu jari dan gangguan vibrasi yang paling banyak terjadi di
telapak kaki. Selain itu secara elektroneurofisiologis ternyata neuropati kusta dapat
terjadi di ekstremitas maupun di wajah.
Di ektremitas saraf yang sering mengalami
gangguan yaitu N. Peroneus Superfisialis,
dan N. Suralis, sedangkan pada wajah yaitu
N. Trigeminal dan N. Fasialis.
Beberapa polineuropati dapat menjadi tidak
jelas polanya karena superimposed dengan
mononeuropati atau mononeuropati multipleks, contoh yang paling sering yaitu
sindrom terowongan karpal pada polineuropati diabetes. Neuropati dapat juga dibagi
berdasar distribusinya, yaitu: polineuropati simetrik distal, polineuropati simetrik
proksimal, polineuropati dengan predominasi ·
ekstremitas atas, distribusi kompleks, keterlibatan saraf kranial, serta neuropati fokal
dan multifokal.
Polineuropati dengan distribusi gangguan
motor dan sensorik distal simetrik merupakan pola paling umum dan banyak ditemui.
Gejala motor ditandai dengan kelemahan
dan atrofi yang dimulai dari ekstremitas
bagian distal kemudian menyebar ke proksimal. Gejala sensorik ditandai dengan adanya
pola distribusi "stocking-and-glove': yaitu seolah-olah membentuk sarungtangan dan kaos
kaki, sehingga pasien merasa perabaannya
berkurang di daerah yang tertutupi "sarung
tangan" dan "kaoskaki"yangtaknampakmata
ini Pola distribusi ini disebabkan karena
saraf yang paling panjang akan mengalami
gangguan terlebih dahulu (length-dependent
polyneuropathy). Pada ekstremitas bawah N.
Tibialis Anterior dan M. Peroneus biasanya
akan terganggu terlebih dahulu dibandingkan bagian posterior betis karena panjang
saraf yang mensarafi bagian anterior betis
lebih panjang dibandingkan bagian posterim: Pola distribusi seperti ini dapat ditemukan pada Charcot-Marie-toothfhereditary
motor and sensory neuropathy (HMSN) tipe
I. Polineuropati simetrik distal yang hanya
mempengaruhi komponen sensorik juga
sering ditemukan pada polineuropati dia-
. betik tahap awal.
Contoh polineuropati simetrik proksimal
yang paling umum yaitu sindrom Guillain-Barre (SGB) dan chronic inflammatory
demyelinating polyneuropathy (CIDP) yang
dibahas dalam bab tersendiri. Diagnosa
lain yang perlu dipikirkan dengan distribusi
seperti ini yaitu porfiria, spina muskular
atrofi, dan penyakit Tangier.
Polineuropati dengan predominasi ektremitas atas dengan gejala sensorik banyak terjadi pada tahap awal kekurangan vitamin
812. Distribusi ini dengan gejala motorik
kadang juga terjadi pada beberapa SGB,
porfiria, dan HMSN. Neuropati dengan keterlibatan saraf kranial dapat disebabkan
668
oleh sarkoidosis, diabetes melitus, dan yang
paling sering yaitu neuropati pada saraf
fasialis yang dikenal dengan Bell's palsy.
Bell's palsy dapat disebabkan berbagai faktor seperti imunologi, infeksi, vaskuler, dan
paling banyak yaitu idiopatik.
PENGOBATAN
PENGOBATAN neuropati sesuai dengan etiologinya. Pemeriksaan penunjang dibutuhkan sebelum memulai terapi definitif.
1. Pemeriksaan Elektrodiagnostik
Pemeriksaan elektrodiagnostik terdiri
dari KHS dan elektromiografi (EMG),
yang standar untuk pemeriksaan neuropati akibat kerusakan serabut sarafbesar.
EMG dapat membedakan antara polineuropati dengan miopati, neuronopati,
pleksopati, ataupun poliradikulopati.
Sebagai kepanjangan pemeriksaan fisik,
pemeriksaan elektrodiagnostik meningkatkan ketajaman distribusi disfungsi saraf,
membedakan keterlibatan motor dan sensorik, tingkat keparahan. Lebih dalam lagi,
elektrodiagnostik dapat menilai gangguan sarafberdasar aksonopati maupun mielinopati. Elektrodiagnostik juga
dapat dilakukan berulang untuk tujuan
evaluasi atau menilai progresifitas penyakit.
2. Biopsi Saraf dan Biopsi Kulit
Biopsi saraf dilakukan untuk mencari
etiologi, lokasi patologi, dan tingkat kerusakan saraf. Dalam beberapa dekade
belakang, biopsi saraf sudah jarang dilakukan karena perkembangan elektrodiagnostik, laboratorium, dan tes genetik.
Saat ini pemeriksaan biopsi saraf dilakukan hila etiologi tidak dapat ditemukan
setelah berbagai pemeriksaan tambahan
dilakukan.
Lain halnya dengan biopsi saraf, biopsi
kulit meningkat secara dramatis dalam
dua dekade belakangan. Biopsi ini menjadi
pemeriksaan baku emas untuk menilai
inervasi serabut saraf kecil intraepidermal tidak bermielin yang menghantarkan
sensasi nyeri dan suhu dari kulit serta berperan dalam regulasi fungsi otonom. Neuropati serabut saraf kecil ini dapat hanya
mempunyai gejala klinis minimal dan
mungkin saja terlewatkan pada pemeriksaan klinis, oleh karena pemeriksaan elektrodiagnostik konvensional hanya dapat
menilai serabut sarafbesar.
3. Pemeriksaan Laboratorium dan Genetik
Pemilihan pemeriksaan laboratorium dan
genetik memberi tantangan tersendiri.
Banyak sekali pemeriksaan yang dapat
dilakukan, namun karena mahal, perlu
Analisa mendalam berdasar anamnesis
dan pemeriksaan fisik sebelum menentukan pilihan yang tepat. Pemeriksaan standar yang disarankan American Academy of
Neurology (AAN) di antaranya gula darah
puasa, elektrolit, pemeriksaan fungsi ginjal,
fungsi hepar, darah lengkap, hitung jenis,
kadarvitamin B12, laju endap darah, fungsi
tiroid, dan jika memungkinkan immunofixation electrophoresis (IFE).
Pemeriksaan . toleransi gula 2 jam
pascapuasa lebih sensitif dibandingkan
dengan pemeriksaan hemoglobin Ale
(HbAlc) dan gula darah puasa Oleh karena
itu pemeriksaan ini perlu dipikirkan jika
pemeriksaan awal normal. Defisiensi vitamin B12 merupakan pemicu neuropati
yang mudah diterapi. Di Indonesia karena
669
Neuropati
pemeriksaan ini lebih mahal dibandingkan
obatnya, maka pemeriksaan ini jarang dilakukan.
Jika dicurigai suatu neuropati demielinisasi, pertimbangkan untuk memeriksa
anti-myelin-associated glycoprotein (antiMAG). Jika dicurigai suatu multifocal motor neuropathy (MMN) pertimbangkan
pemeriksaan anti-GM1. Pada varian SGB
diperiksakan antiGQlb, antiGM1, dan
antiGD-la. Untuk kecurigaan etiologi infeksi sistemikjgangguan imunitas, perlu
dilakukan pemeriksaan cairan serebrospinal. Pasien perokok rentan terhadap
keganasan. Jika didapatkan neuropati
sensorik pada perokok, pertimbangkan
pemeriksaan antibodi antiHu, yang berhubungan dengan neuropati paraneoplastik.
Pemeriksaan genetik merupakan pemeriksaan lanjutan jika dicurigai neuropati
herediter secara klinis ditunjang dengan
klasifikasi menurut elektrodiagnostik.
Pemeriksaan ini dapat dilakukan dengan
lebih efisien secara bertahap dimulai
dari kecurigaan klinis paling besar dan
paling sering terjadi.
CONTOH-CONTOH NEUROPATI
1. Inherited Peripheral Neuropathy I
Charcot-Marie-Tooth
Salah satu etiologi neuropati perifer
yaitu mutasi genetik yang diturunkan
dari orang tua ke anaknya. Neuropati
herediter (inherited neuropathy) sering
disebut dengan penyakit Charcot-MarieTooth (CMT). Nama ini diberikan sebagai
penghormatan tiga orang yang pertama
kali mendeskripsikan penyakit ini pada
tahun 1886. Sebagian besar CMT meru
pakan neuropati motorik dan sensorik,
oleh karena itu sering juga disebut
dengan hereditary motor and sensory
neuropathy (HMSN).
CMT dibagi menjadi dua: CMT 1 yang memiliki patologi hypertrophic demyelinating neuropathy dan ada perlambatan
KHS ( <38m/s pada ekstremitas atas); dan
CMT 2 yang memiliki patologi degenerasi
aksonal dengan KHS yang relatif normal.
Untuk menDiagnosa pasien neuropati
herediter kadang cukup mudah. Jika pasien
memiliki kelemahan ektremitas bagian
distal disertai hilangnya fungsi sensorik,
pes cavus, pemeriksaan KHS dengan
hasil melambat, dan riwayat keluarga
yang cukup kuat, maka pasien ini
kemungkinan dapat menderita CMT. Di
sisi lain, mungkin saja neuropati herediter
mwicul sebagai de novo atau baru muncul
ketika dewasa
Pada CMT ada 44 lokus di 50 gen
yang dapat bermutasi yang memicu kelainan ini, sehingga gejala klinisnya cukup kompleks dengan pola yang
bervariasi membuat tes genetik menjadi mahal. Pemeriksaan genetik yang
efisien dapat dilakukan dengan memilah
kemungkinan jenis CMT berdasar
pemeriksaan elektrodiagnostik.
2. Neuropati Diabetes
Diabetes melitus (DM) merupakan salah
satu pemicu terbanyak neuropati perifer di dunia. Lebih dari setengah pasien
diabetes mengalami neuropati, dan
setengah orang yang memiliki neuropati
yaitu pasien diabetes.
Perubahan patologi sarafyang paling be-
670
sar pada neuropati diabetes terjadi pada
serabut saraf perifer di distal, namun
kerusakan ini dapat juga terjadi
pada proksimal, baik di ganglion radiks
dorsalis ataupun di kornu anterior. ada beberapa teori mekanisme pemicu neuropati diabetes, antara lain
gangguan vaskular, hipotesis metabolik,
perubahan sintesis protein dan transpor
aksonal, serta mekanisme imunologi.
Berbagai mekanisme ini memicu
bentuk-bentuk neuropati yang beragam
pula, baik neuropati sensorik, otonom,
fokal, multifokal, simetrik, maupun polineuropati.
Gangguan vaskular diprediksi dapat memicu penebalan dinding pembuluh
darah mikro dan memicu iskemia
pada vasa neuron urn. Berbagai penelitian
telah mendukung teori ini, mulai dari studi
in vitro, in vivo pada tikus, serta otopsi
dan biopsi pada N. Suralis. Studi pada
tikus STZ-diabetes menunjukkan penurunan oksigenasi jaringan dan peningkatan
resistensi vaskular. Lesi multifokal pada
jaringan biopsi dan otopsi manusia juga
konsisten dengan teori bahwa diabetes
memicu iskemik pada jaringan
saraf perifer.
Hipotesis metabolik tentang hiperglikemia berdasar studi retrospektif yang
menyatakan bahwa komplikasi neuropati pada diabetes yang lebih dini dan
lebih berat berhubungan dengan kontrol glikemik yang buruk. Di sisi lain,
acute painful diabetic neuropathy juga
membaik dengan penurunan berat badan
dan kontrol glikemik yang baik. Hal ini sangat mungkin terjadi karena pada
kondisi hiperglikemia, perubahan sintesis
protein dan transpor aksonal akan mengganggu transpor makromolekul dari akson
di distal kembali ke zona perinuklear
untuk didaur ulang. Gangguan ini memicu degenerasi aksonal di distal.
PENGOBATAN neuropati diabetik sangat
beragam. Oleh karena sifatnya yang
sistemik, maka PENGOBATAN yang dilakukan harus menyeluruh tidak berhenti
sampai pengobatan saja, namun juga
evaluasi sepanjang perjalanan penyakit. Pasien diabetes perlu dinilai sensibilitas daerah distal. Pasien yang tidak
dapat merasakan tes monofilamen lOg
kemungkinan memiliki Diagnosa polineuropati distal simetrik dan cenderung
akan mengalami ulserasi pada telapak
kakinya. Oleh karena itu pasien perlu dilakukan tindakan pencegahan dengan edukasi serta pemakaian alas kaki yang sesuai,
atau dirujuk ke ahli kaki (podiatrist).
Pasien diabetes juga rentan terhadap
gangguan saraf otonom. Jika ada
riwayat hipotensi ortostatik, presinkop,
dan basil pemeriksaan EKG-treadmill
menunjukkan gambaran intoleran, kemungkinan pasien mengalami cardiac
dysautonomia. Keadaan ini dapat meningkatkan risiko kematian menjadi
2 sampai 5 kali lipat, antara lain akibat
painless myocardial infarct jika pasien
mengalami kelelahan yang hebat dan
tiba-tiba disertai kulit yang pucat, mual,
kebingungan, sesak napas, atau batuk.
Disfungsi ereksi sebagai salah satu
gangguan otonom dapat terjadi pada
pasien DM. Jika didapatkan disfungsi
671
Neuropati
ereksi maka tidakmenutup kemungkinan
ada penyakit kardiovaskular lainnya
yang terkait dengan gangguan otonom.
Oleh karena itu perlu dilakukan evaluasi
jantung menyeluruh pada pasien DM
dengan gangguan disfungsi ereksi.
Diabetes juga meningkatkan risiko berbagai jenis neuropati lainnya. Diabetes
meningkatkan risiko reaktivasi herpes
zoster dan painful thoracic radiculopathy.
Baal kedua tangan pada pasien diabetes
juga masih sangat mungkin karena CTS
atau carpal tunnel syndrome bilateral.
PENGOBATAN neuropati diabetes yaitu
dengan kontrol gula darah yang baik
mendekati normoglikemia atau kadar
HbAlc dipertahankan di bawah 7%. Bila
ada nyeri, maka obat simptomatik
pilihan diantaranya yaitu gabapentin,
pregabalin, karbamazepin, maupun okskarbazepin. Obat-obat antinyeri neuropatik ini dapat dikombinasikan dengan
obat anti inflamasi nonsteroid (OAINS),
analgesik lainnya, ataupun antidepresan.
Namun perlu diingat karena OM yaitu
penyakit sistemik, interaksi obat dan
fungsi ginjal perlu diperhatikan sebelum
terapi diberikan.
3. Bell's Palsy
Merupakan kelainan saraf fasialis tipe
perifer idiopatik dan pemicu terbanyak
lesi nervus fasial unilateral yang dapat
mengenai semua jenis kelamin dan usia.
Prevalensinya sekitar 23 per 100.000
penduduk dan diperkirakan meningkat
pada pasien DM, hipertensi, serta ibu
hamil masa perinatal.
Walaupun Bell's palsy diperkirakan
idio-atik, namun sebenarnya kurang
tepat karena studi mengaitkannya dengan
infeksi herpes simplex virus (HSV)-1. Pacta
autopsi kasus ini, HSV-1 dapat diisolasi
dari ganglion genikulatum serta terdeteksi
pacta cairan endoneurium sebagian besar pasien dibandingkan dengan kontrol
sehat. Pacta sindrom Ramsay-Hunt dapat
diisolasi virus varicella zoster.
Pacta Bell's palsy terjadi inflamasi yang memicu demielinisasi segmental, bahkan dapat terjadi kerusakan aksonal, sehingga terjadi kelainan nervus fasialis tipe
perifer yang mencapai maksimal dalam
48-72 jam pascaonset. Abnormalitas dapat
terjadi pacta lokasi sepanjang perjalanan
nervus fasialis sejak keluar dari inti nervus
fasialis di pons hingga serabut terminalnya
yang menginervasi efektor. Lokasi lesi terbanyak di bagian proksimal kanalis fasialis
yang merupa-kan tempat tersempit.
Nyeri pacta area belakang aurikular
dapat muncul 1-2 hari sebelum onset.
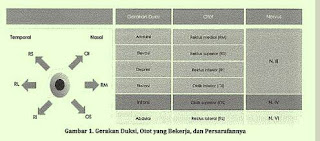
Level kerusakan nervus fasialis menentukan manifestasi klinis yang muncul. Nervus fasialis memiliki bagian motorik dan
sensorik (Gambar 2), maka gangguannya
dapat berupa kelumpuhan otot fasialis
ipsilateral (muskulus frontalis, orbikularis okuli, bucinator; orbikularis oris, dan
platisma), penurunan lakrimasi ipsilateral, hiperakusis (muskulus stapedius)
ipsilateral, penurunan sali-vasi ipsilateral,
dan penurunan indera pengecap ipsilateral pacta duapertiga anterior lidah (rasa
manis, asam, dan asin). Pacta beberapa
kasus juga dapat disertai hipestesi pacta
satu atau lebih cabang nervus trigeminal.
Derajat kelumpuhan nervus fasialis dinilai memakai sistem grading HouseBrackmann yang membagi manifestasi
klinis menjadi 6 derajat (Tabel 2)
Diagnosa Bell's palsy ditegakkan secara
klinis. Pada pemeriksaan MRI dengan kontras, didapatkan penyangatan nervus fasialis
yang merepresentasikan inflamasi. Cairan
serebrospinal menunjukkan peningkatan
ringan limfosit dan monosit. Pemeriksaan
elektrofisiologi, yaitu refleks kedip (blink
reflex) dapat menentukan topis kerusakan
nervus fasialis. Pemeriksaan ini dilakukan
setelah onset 14 hari, karena pada <14 hari
pascaonset masih terjadi kerusakan nervus
673
fasialis, sehingga belum dapat diperkirakan derajat kerusakan akhirnya. Diagnosa
banding kasus ini yaitu penyakit Lyme,
otitis media, sindrom Ramsay-Hunt, sarkoidosis, SGB, tumor kelenjar parotis, multipel
sklerosis, stroke, dan tumor.
lnflamasi pada nervus fasialis dapat diatasi
dengan pemberian glukokortikoid oral,
yaitu prednison 40-60mg perhari selama 10
hari dengan penurunan dosis bertahap. Jika
diduga infeksi virus sebagai etiologinya, dapat
ditambahkan antiviral, yaitu asiklovir 400mg 5
kali sehari selama 7 hari atau valasiklovir 1g 3
kali sehari selama 7 hari dalam wa























.jpeg)

.jpeg)
